G.N.刘易斯和M.伦道尔在1921年定义离子强度I为:
![]()
式中mi为电解质溶液中i离子的质量摩尔浓度, Zt为该离子价数, 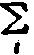 为各种 离子的miZ2i求和。
为各种 离子的miZ2i求和。
由于体积摩尔浓度C与质量摩尔浓 度m的关系为
C=mρ/(1+0.001mM)
M为电解质的分子量,ρ为溶液密度。于是,在稀水溶液中:
![]()
计算离子强度时,必须用离子的真实浓度; 当为弱电解质溶液时,离子真实浓度为电解质浓度与其电离度的乘积。
离子强度表征着溶液中离子所经受的平均电荷强度及不同组成的溶液的离子环境的一种重要的物理化学参量。
对于象海水这样的复杂的电解质溶液体系,其离子强度无法按定义式计算,常利用下列一些经验公式求算:
I=35.9997Cl/(1000-1.81578Cl)=19.9273S/(1000-1.005109S )式中Cl为海水氯度,S为海水盐度,I为离子强度,其单位为质量摩尔浓度。如果使用其他单位则需进行浓度换算。
J.P.赖利曾提出一个更简单的海水离子强度经验公式:
I=0.020S
式中I为质量摩尔浓度单位。
M.惠特菲尔德1971年提出可按下列经验公式计算以体积摩尔浓度为单位的海水离子强度:
I=0.019S
因此,对于盐度为35的海水,其离子强度若以质量摩尔浓度为单位应为0.70;而若以体积摩尔浓度为单位,则为0.67。
刘易斯和伦道尔发现,在具有相同离子强度的所有稀溶液中,给定强电解质的活度系数大致相同,与存在的离子本性无关。这就是离子强度原理。后来德拜-许克尔理论阐明了该原理(见德拜-许克尔理论)。
在海洋化学中研究海水化学模型时,R.M.派特科威茨等1969年曾提出了一种有效离子强度Ie的概念,它是根据如下定义:

式中[i]是海水中自由离子的体积摩尔浓度,[P]是海水中离子对的体积摩尔浓度,Zi,Zp分别为自由离子的价数和离子对的净电荷数。同时,他们还曾提出有效离子强度原理: 海水中自由离子的活度系数仅依赖于海水有效离子强度,而与离子组成无关。