8-N rule
简介
又称Hume-Rothery (8-N) 规
则。在N族元素所形成的共价键结构
中,每个原子应有(8-N)个近邻,并
由此决定晶体结构。周期表中Ⅳ-Ⅵ
(B)族元素的典型晶体结构,基于8
电子壳层 (惰性气体组态) 的高稳定
性。为了形成8电子壳层,一个4价的
原子要与4个最近邻组成共价键,一
个5价的原子要与3个最近邻键合,
一个6价的原子要与2个最近邻键合
等。在Ⅳ族元素中,C、Si、Ge(以及
灰锡)具有金刚石型的结构,其中每个
原子都被另外4个原子所形成的四面
体所包围,如图所示。每个晶胞平均占
有8个原子,其中4个分配在正常面
心立方结构的阵点上; 另外4个则交
叉配置在晶胞内部8个四面体间隙之
内的中心位置,这正相当于面心立方
结构的每个阵点上,各配置2个原子,
或者看成是由2个面心立方点阵沿
〈111〉方向相对错动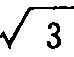 a/4穿插而
a/4穿插而
成。在Ⅴ族中,As、Sb、Bi等为菱形
晶体结构,可由简单立方通过变形,使
每个原子只有3个最近邻。Ⅵ族的Se
和Te有三角链式结构,最近邻数为
2。对于正常价金属间化合物CmAn,亦
符合 (8-N) 规则,即mec=n (8-
eA),其中ec、e A分别为正、负离子的
价电子数。例如,Ⅲ-Ⅴ族及Ⅱ-Ⅵ族化
合物构成的内锌矿和纤锌矿也属于金
刚石结构。其中,一半的原子(Ⅲ族或
Ⅱ族)组成面心立方亚点阵,另一半的
原子(Ⅴ族或Ⅵ族)也组成面心立方亚
点阵,每个原子的平均电子数是4,对
于整个化合物来讲,也符合(8-N)规
则。
