5.2.1 一般结构 5.2.1.1 结构和分类 α-氨基酸是蛋白质的基本构成单位。这些氨基酸含有一个α-碳原子,并与一个氢原子、一个氨基、一个羧基和一个侧链R基共价连接。

天然存在的蛋白质含有21种不同的基本氨基酸,它们彼此通过酰胺键相连接。第21种新的氨基酸,已经被认定是一种天然氨基酸,为硒代半胱氨酸[12]。这些氨基酸的差别仅在于含有化学性质不同的侧链R基团(图5.1)。氨基酸的物理化学性质,如净电荷、溶解度、化学反应性和氢键形成能力,取决于R基团的化学性质。 图5.1所示为氨基酸具有遗传密码(包括硒代半胱氨酸),即每一种氨基酸具有一个独特的t-RNA,能将m-RNA的遗传信息转译成蛋白质合成中的一个氨基酸顺序。除了在图5.1中列举的21种基本氨基酸外,一些蛋白质还含有其他类型的氨基酸,它们是基本氨基酸的衍生物。这些衍生氨基酸或者是交联氨基酸,或者是单个氨基酸的简单衍生物。含有衍生氨基酸的蛋白质被称为结合蛋白质。存在于大多数蛋白质中的胱氨酸是交联氨基酸的一个很好的例子。其他交联氨基酸,如锁链素、异锁链素和二、三酪氨酸也被发现存在于结构蛋白质中,如弹性蛋白和节枝弹性蛋白。几种氨基酸的简单衍生物存在于一些蛋白质中,例如,4-羟基脯氨酸和5-羟基赖氨酸存在于胶原蛋白,它们是在胶原纤维成熟过程中后转译修饰的结果。磷酸丝氨酸和磷酸苏氨酸存在于一些蛋白质中,其中包括酪蛋白。N-甲基赖氨酸存在于肌球蛋白,而γ-羧基谷氨酸存在于几种血凝固因子和钙结合蛋白质中。

图5.1 存在于蛋白质中的基本α-氨基酸 在括号中显示了各氨基酸的三个或一个字母代码。同时也显示了每一种氨基酸的mRNA密码子

5.2.1.2 氨基酸的立体化学 除Gly外,所有氨基酸的α-碳原子都是不对称的,即有四个不同的基团与它相连接。由于此不对称中心,氨基酸显示光学活性,即它们能转动线性偏振光平面。Ile和Thr除了含有不对称的α-碳原子外,它们分子中的β-碳原子也是不对称的,因此Ile和Thr都有四个对映体。在衍生氨基酸中,羟基脯氨酸和羟基赖氨酸也含有两个不对称碳原子。在天然存在的蛋白质中,仅含有L-氨基酸。L-和D-对映体可用下式表示:

上述命名是基于D-和L-甘油醛构型,而不是根据线性偏振光实际转动的方向。这就是说,L-构型并非指左旋(L-甘油醛是左旋),事实上大多数L-氨基酸为右旋而非左旋。 5.2.1.3 氨基酸的酸碱性质 由于氨基酸同时含有羧基(酸性)和氨基(碱性),因此它们既有酸也有碱的性质,即它们是两性电解质。例如,最简单的氨基酸Gly受溶液pH的影响可能有3种不同的离解状态:
![]()
在中性pH范围,α-氨基和α-羧基都处在离子化状态,此时氨基酸分子是偶极离子或两性离子。偶极离子以电中性状态存在时的pH被称为等电点(pI)。当两性离子被酸滴定时,—COO–基质子化,当—COO–和—COOH的浓度相等时的pH被称为pKa1(即酸离解常数Ka1的负对数)。与此类似,当两性离子被碱滴定时,—NH+3基去质子化,当—NH+3和—NH2浓度相等时的pH被称为pKa2。图5.2所示为偶极离子典型的电化学滴定曲线。除α-氨基和α-羧基外,Lys、Arg、His、Asp、Glu、Cys和Tyr的侧链也含有可离子化的基团。表5.1所示为氨基酸中所有可离子化基团的pKa值。根据下式可以从氨基酸的pKa1、pKa2和pKa3值估计等电点。

图5.2 一种典型氨基酸的滴定曲线
侧链不含有带电荷基团的氨基酸,pI=(pKa1+pKa2)/2 酸性氨基酸,pI=(pKa1+pKa3)/2 碱性氨基酸,pI=(pKa2+pKa3)/2 下标1、2和3分别代表α-羧基、α-氨基和侧链上可离子化的基团。
表5.1 在25℃时,游离氨基酸中可离子化基团的性质
| 氨基酸 | pK·a1(-COOH) | pK·a2 (-NH+3) | pKa3(侧链) | pI |
| 丙氨酸 | 2.34 | 9.69 | – | 6.00 |
| 精氨酸 | 2.17 | 9.04 | 12.48 | 10.76 |
| 天冬酰胺 | 2.02 | 8.80 | – | 5.41 |
| 天冬氨酸 | 1.88 | 9.60 | 3.65 | 2.77 |
| 半胱氨酸 | 1.96 | 10.28 | 8.18 | 5.07 |
| 谷氨酰胺 | 2.17 | 9.13 | – | 5.65 |
| 谷氨酸 | 2.19 | 9.67 | 4.25 | 3.22 |
| 甘氨酸 | 2.34 | 9.60 | – | 5.98 |
| 组氨酸 | 1.82 | 9.17 | 6.00 | 7.59 |
| 异亮氨酸 | 2.36 | 9.68 | – | 6.02 |
| 亮氨酸 | 2.30 | 9.60 | – | 5.98 |
| 赖氨酸 | 2.18 | 8.95 | 10.53 | 9.74 |
| 蛋氨酸 | 2.28 | 9.21 | – | 5.74 |
| 苯丙氨酸 | 1.83 | 9.13 | – | 5.48 |
| 脯氨酸 | 1.94 | 10.60 | – | 6.30 |
| 丝氨酸 | 2.20 | 9.15 | – | 5.68 |
| 苏氨酸 | 2.21 | 9.15 | – | 5.68 |
| 色氨酸 | 2.38 | 9.39 | – | 5.89 |
| 酪氨酸 | 2.20 | 9.11 | 10.07 | 5.66 |
| 缬氨酸 | 2.32 | 9.62 | – | 5.96 |
在蛋白质分子中,一个氨基酸的α-COOH通过酰胺键与相邻氨基酸的α-NH2相结合,于是,蛋白质分子中可以离子化的基团为N-末端氨基、C-末端羧基和侧链上可离解的基团。在蛋白质分子中,这些可离子化的基团的pKa1不同于它们在游离氨基酸中相应的数值(表5.2)。与游离氨基酸相比,pKa的改变与蛋白质中这些基团可改变的电子与电介质环境有关(这一特性在酶中至关重要)。 根据Henderson-Hasselbach方程可以计算一个基团在任何指定的溶液pH下的离子化程度:
![]()
根据此式测定各个可离子化基团的离子化程度,然后将总的负电荷和正电荷相加,可估计一种蛋白质在指定pH下的净电荷。 根据侧链与水相互作用的程度可将氨基酸分成几类。含有脂肪族(Ala、Ile、Leu、Met、Pro和Val)和芳香族(Phe、Trp、和Tyr)侧链为疏水性氨基酸,因此它们在水中的溶解度有限(表5.3)。极性(亲水)氨基酸易溶于水,它们或者带有电荷(Arg、Asp、Glu、His和Lys),或者不带有电荷(Ser、Thr、Asn、Glu和Cys)。Arg和Lys的侧链分别含有胍基和氨基,因此在中性pH带正电荷(为碱性氨基酸)。虽然His的咪唑基具有碱性的性质,然而在中性条件下它仅略带正电荷。Asp和Glu的侧链含有一个羧基,因此在中性pH条件下,这些氨基酸带有一个净负电荷。碱性和酸性氨基酸具有很强的亲水性。在生理条件下,一种蛋白质的净电荷取决于它分子中碱性和酸性氨基酸残基的相对数目。
表5.2 蛋白质可离子化基团的平均pKa
| 可离子化基团 | pKa | 酸形式↔碱形式 |
| 末端COOH 末端NH2 侧链COOH (Glu,Asp) 侧链NH2 | 3.75 7.8 4.6 10.2 | —COOH↔—COO– —NH+3↔—NH2 —COOH↔—COO– —NH+3↔—NH2 |
| 咪唑基 | 7.0 | 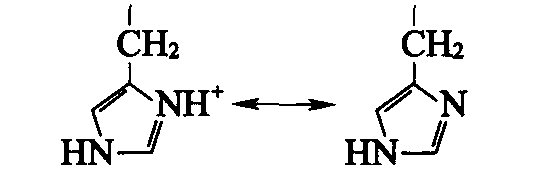 |
| 巯基 | 8.8 | —SH↔—S– |
| 酚羟基 | 9.6 | 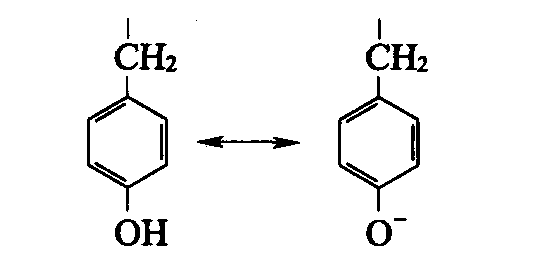 |
| 胍基 | >12 | 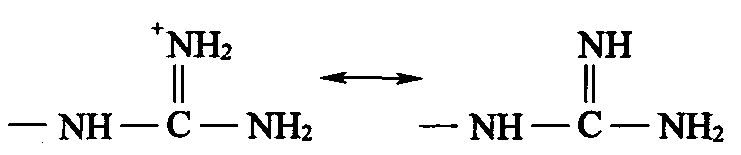 |
表5.3 氨基酸的性质(25℃)
| 氨基酸 | 相对分子质量 | 残基体积 △3 | 残基面积 △2 | 溶解度/(g/L) | 疏水性/(kcal/mol)* (△G0tr) |
| 丙氨酸 精氨酸 天冬酰胺 天冬氨酸 | 89.1 174.2 132.1 133.1 | 89 173 111 114 | 115 225 150 160 | 167.2 855.6 28.5 5.0 | 0.4 -1.4 -0.8 -1.1 |
| 半胱氨酸 | 121.1 | 109 | 135 | – | 2.1 |
| 谷氨酰胺 谷氨酸 甘氨酸 | 146.1 147.1 75.1 | 144 138 60 | 180 190 75 | 7.2(37℃) 8.5 249.9 | -0.3 -0.9 0 |
| 组氨酸 | 155.2 | 153 | 195 | – | 0.2 |
| 异亮氨酸 亮氨酸 赖氨酸 蛋氨酸 苯丙氨酸 脯氨酸 丝氨酸 苏氨酸 色氨酸 酪氨酸 缬氨酸 | 131.2 131.2 146.2 149.2 165.2 115.1 105.1 119.1 204.2 181.2 117.1 | 167 167 169 163 190 113 89 116 228 194 140 | 175 170 200 185 210 145 115 140 255 230 155 | 34.5 21.7 739.0 56.2 27.6 620.0 422.0 13.2 13.6 0.4 58.1 | 2.5 2.3 -1.4 1.7 2.4 1.0 -0.1 0.4 3.1 1.3 1.7 |
注:*△G值是相对于甘氨酸而言,氨基酸侧链在L-辛醇与水之间的分配系数[41]。 不带电荷的中性氨基酸的极性处于疏水氨基酸和带有电荷的氨基酸之间。Ser和Thr的极性可归因于它们含有能与水形成氢键的羟基。既然Tyr也含有一个在碱性条件下能解离的酚羟基,因此可以认为它是一种极性氨基酸。然而,基于其在中性pH条件下的溶解性,它应归于疏水性氨基酸。Asn和Gln的酰胺基能通过氢键与水相互作用。经酸或碱水解,Asn和Gln的酰胺基转变成羧基,同时释放出氨。大多数半胱氨酸残基在蛋白质中以胱氨酸存在,后者是半胱氨酸通过它的巯基氧化形成二硫交联而产生的二聚体。 脯氨酸是一种独特的氨基酸,因为它是蛋白质分子中唯一的一种亚氨基酸。在脯氨酸分子中,丙基侧链通过共价连接的方式同时与α-碳和α-氨基连接形成一个吡咯烷环状结构。 5.2.1.4 氨基酸的疏水性 构成蛋白质的氨基酸残基的疏水性是影响蛋白质和肽的物理化学性质(如结构、溶解度和脂肪结合能力等)的一个重要因素。疏水性可被定义如下:在相同的条件下一种溶于水中的溶质的自由能与溶于有机溶剂的相同溶质的自由能相比所超过的数值。估计氨基酸侧链的相对疏水性的最直接和最简单的方法为实验测定氨基酸侧链溶于水和溶于一种有机溶剂(如辛醇或乙醇)的自由能变化。可采用下式表示一种溶于水的氨基酸的化学势: